EASD糖尿病精准治疗:从「狭路相逢」到「针锋相对」
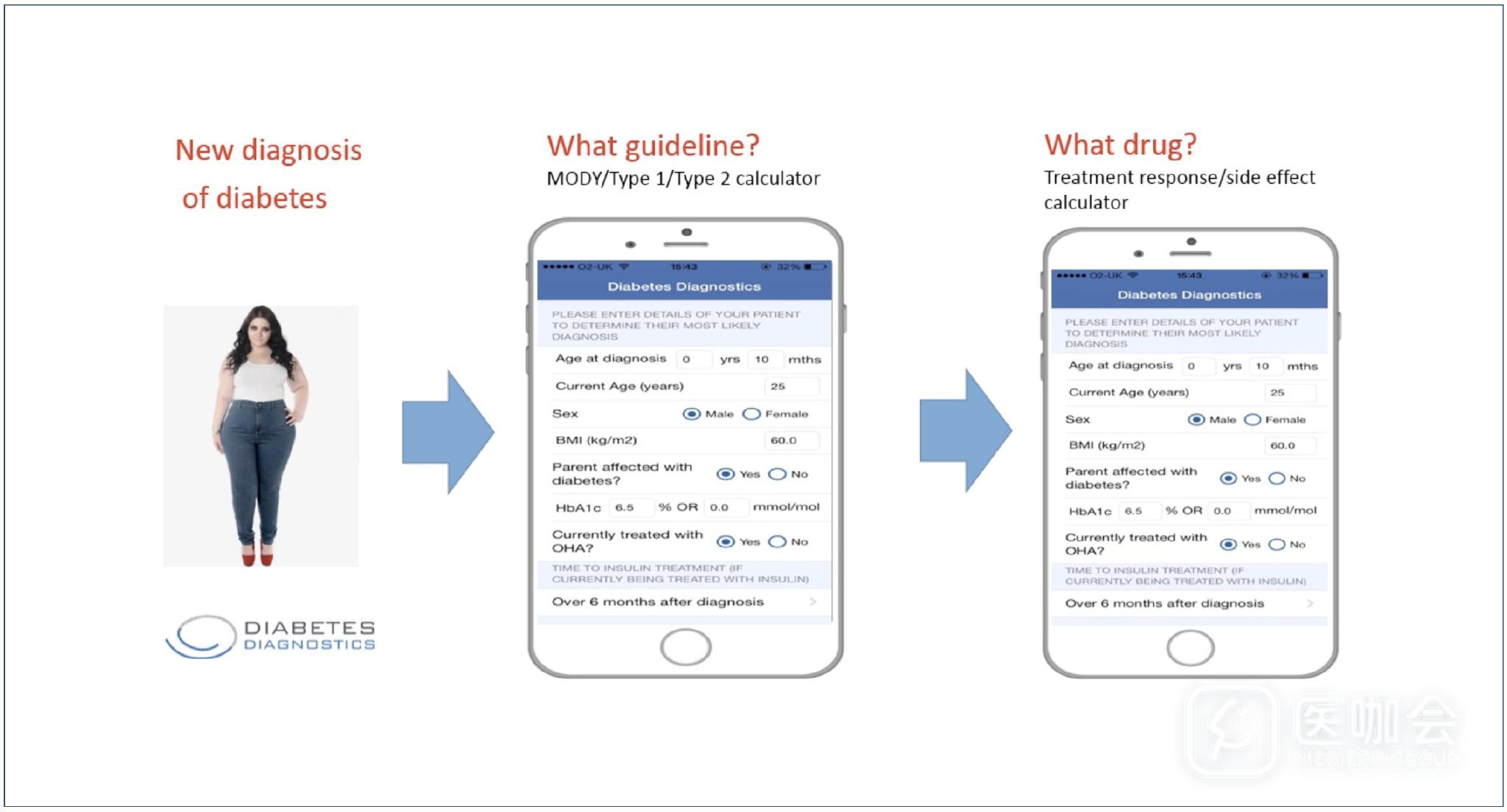
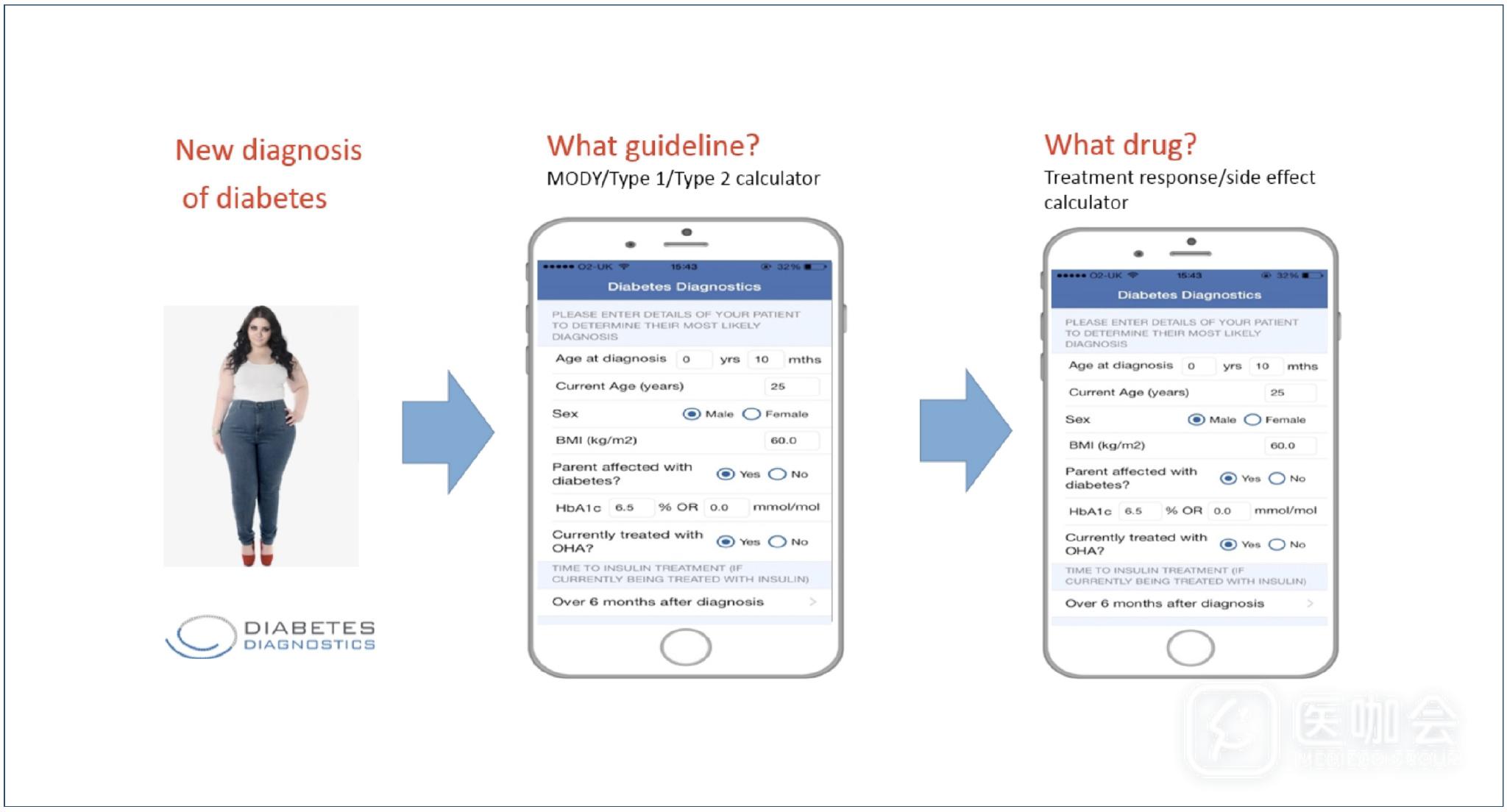
2017年EASD上分别发布了「Precision medicine in common diabetes」和「Clustering of diabetes into novel subgroups provides improved prediction of outcome」二项演讲,前者谈到了如何基于患者的特点,建立一种模型预测哪种治疗对哪种患者疗效以及耐受性最好【如下图】。
后者则谈到糖尿病的五种亚型以及以助于临床结局的预测。研究相关内容均已分别出版在今年的Diabetes care 和 Lancet杂志中。对于两项研究的内容,今年ADA中关于精准医学主题报告中也对此两项研究成果作为范例引经据典【查看详情:糖尿病的精准医学:精彩研究和病例盘点】。
今年的EASD,「Precision medicine in common diabetes」的研究者再次发表演讲,对两种方法进行了更深层次的分析探讨,更准确的说,应该说是对后者进行碾压,当然,只不过方式比较优雅,完全符合英国人一贯的绅士气质。稍后可能会有文章发表,也可能没有,不过「Clustering of diabetes into novel subgroups provides improved prediction of outcome」的研究者对此的回应可能会是:呵呵,你们说的都对,你们是最棒的。
在今年的EASD演讲中,研究者对两种分类方法在以下四个方面进行了分析探讨:
5种亚型的分类是否具有可重复性
亚型分类之间的疾病进展和并发症发生是否不同
亚型分类是否有助于预测药物疗效
相对简单的临床变量【如诊断年龄,性别,BMI,基线HbA1C】在预测结局方面是否要优于亚型分类
2017年EASD上分别发布了「Precision medicine in common diabetes」和「Clustering of diabetes into novel subgroups provides improved prediction of outcome」二项演讲,前者谈到了如何基于患者的特点,建立一种模型预测哪种治疗对哪种患者疗效以及耐受性最好【如下图】。
后者则谈到糖尿病的五种亚型以及以助于临床结局的预测。研究相关内容均已分别出版在今年的Diabetes care 和 Lancet杂志中。对于两项研究的内容,今年ADA中关于精准医学主题报告中也对此两项研究成果作为范例引经据典【查看详情:糖尿病的精准医学:精彩研究和病例盘点】。
今年的EASD,「Precision medicine in common diabetes」的研究者再次发表演讲,对两种方法进行了更深层次的分析探讨,更准确的说,应该说是对后者进行碾压,当然,只不过方式比较优雅,完全符合英国人一贯的绅士气质。稍后可能会有文章发表,也可能没有,不过「Clustering of diabetes into novel subgroups provides improved prediction of outcome」的研究者对此的回应可能会是:呵呵,你们说的都对,你们是最棒的。
在今年的EASD演讲中,研究者对两种分类方法在以下四个方面进行了分析探讨:
- 5种亚型的分类是否具有可重复性
- 亚型分类之间的疾病进展和并发症发生是否不同
- 亚型分类是否有助于预测药物疗效
- 相对简单的临床变量【如诊断年龄,性别,BMI,基线HbA1C】在预测结局方面是否要优于亚型分类
研究者通过使用ADOPT临床研究中的数据进行验证。根据不同变量【GAD抗体,BMI,诊断时年龄,HbA1C,HOMA-β功能,HOMA-IR】进行聚类分析后,将T2DM分成五个亚型。
1. 亚型人群分布及构成
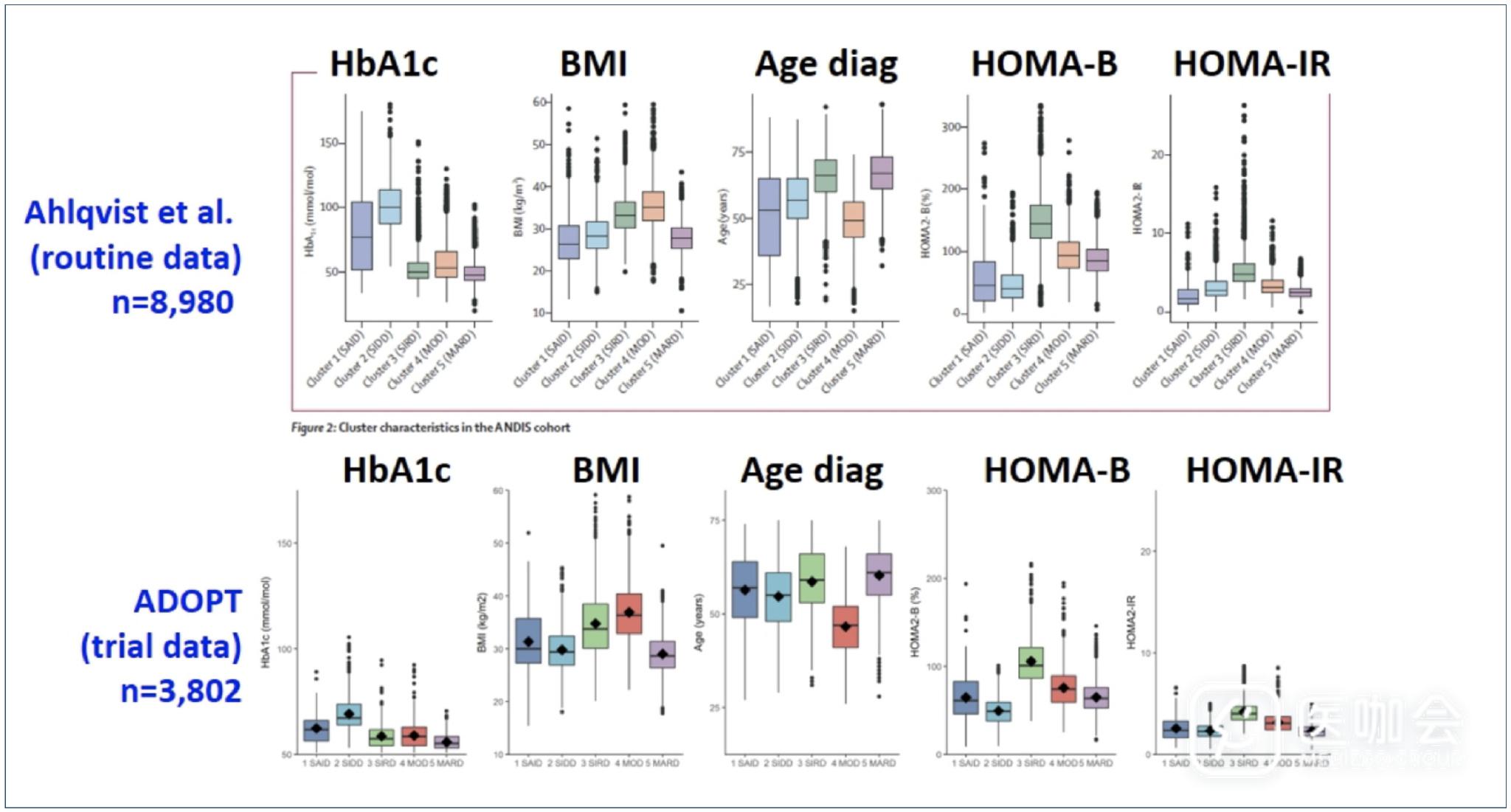
ADOPT研究中五种人群中分布情况,与Ahlqvist教授研究中的分布类似【图1,图2】。
图1. Ahlqvist教授研究和ADOPT研究中亚型人群分布(HbA1C,BMI,Age,HOMA-B,HOMA-IR分层)
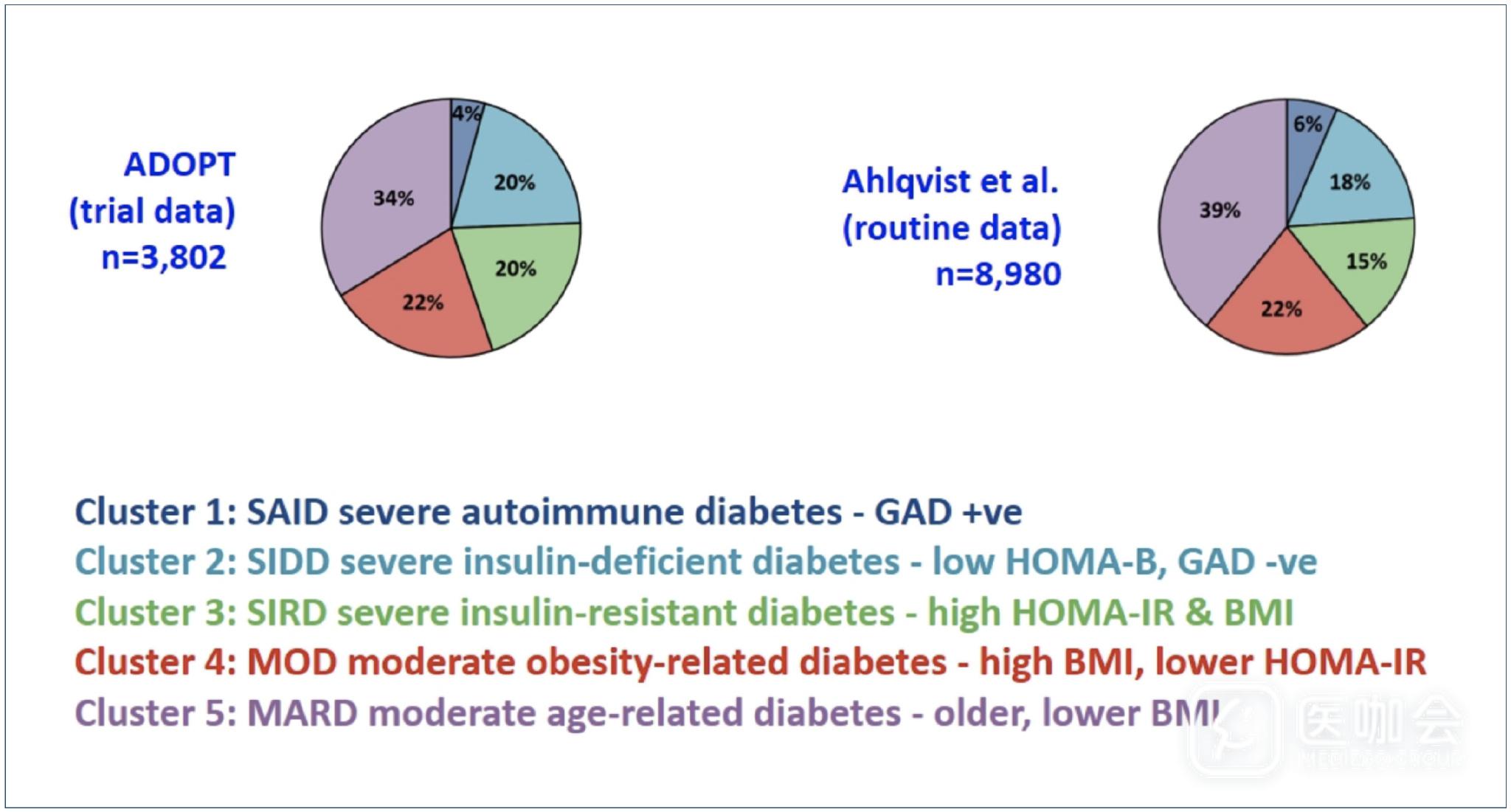
图2. Ahlqvist教授研究和ADOPT研究中亚组人群构成
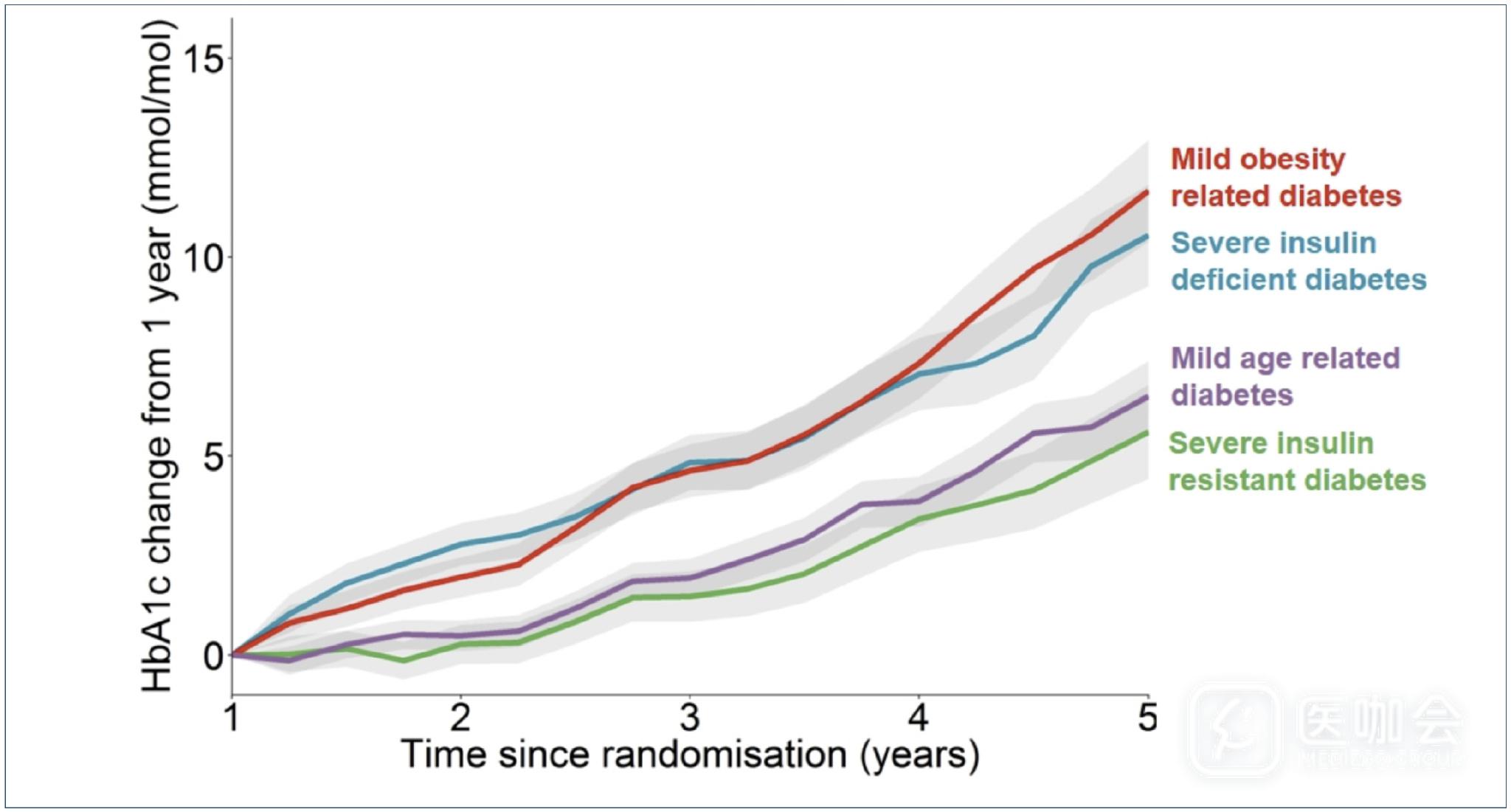
2. HbA1C进展速度比较
在ADOPT研究的分类亚型中,SIRD和MARD二种亚型的HbA1C进展速度更缓慢,且独立于治疗方案【图3】。相比四种亚型分类(未纳入SAD:自身免疫性糖尿病),通过简单的临床指标进行的回归分析的决定系数R2相更高【图4】,说明通过简单的临床指标进行分类更能解释HbA1C变化,而且右图显示通过单个指标分层【诊断年龄】即可区分出HbA1C的进展速度。
图3. ADOPT研究中亚组人群HbA1C进展情况
图4. 基于简单临床指标分层【诊断年龄】各组HbA1C的进展情况
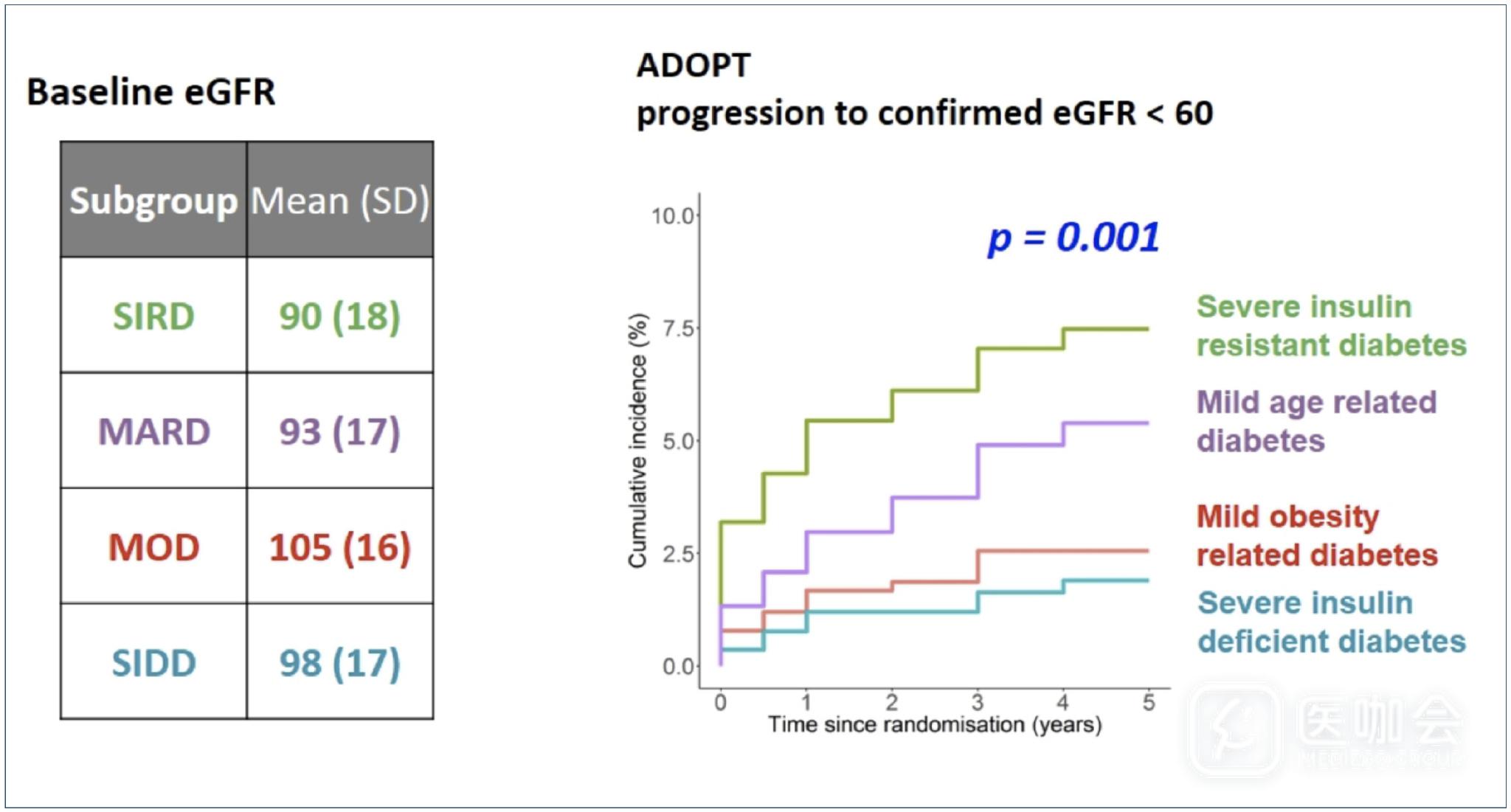
3. 亚型分类各组肾病进展速度
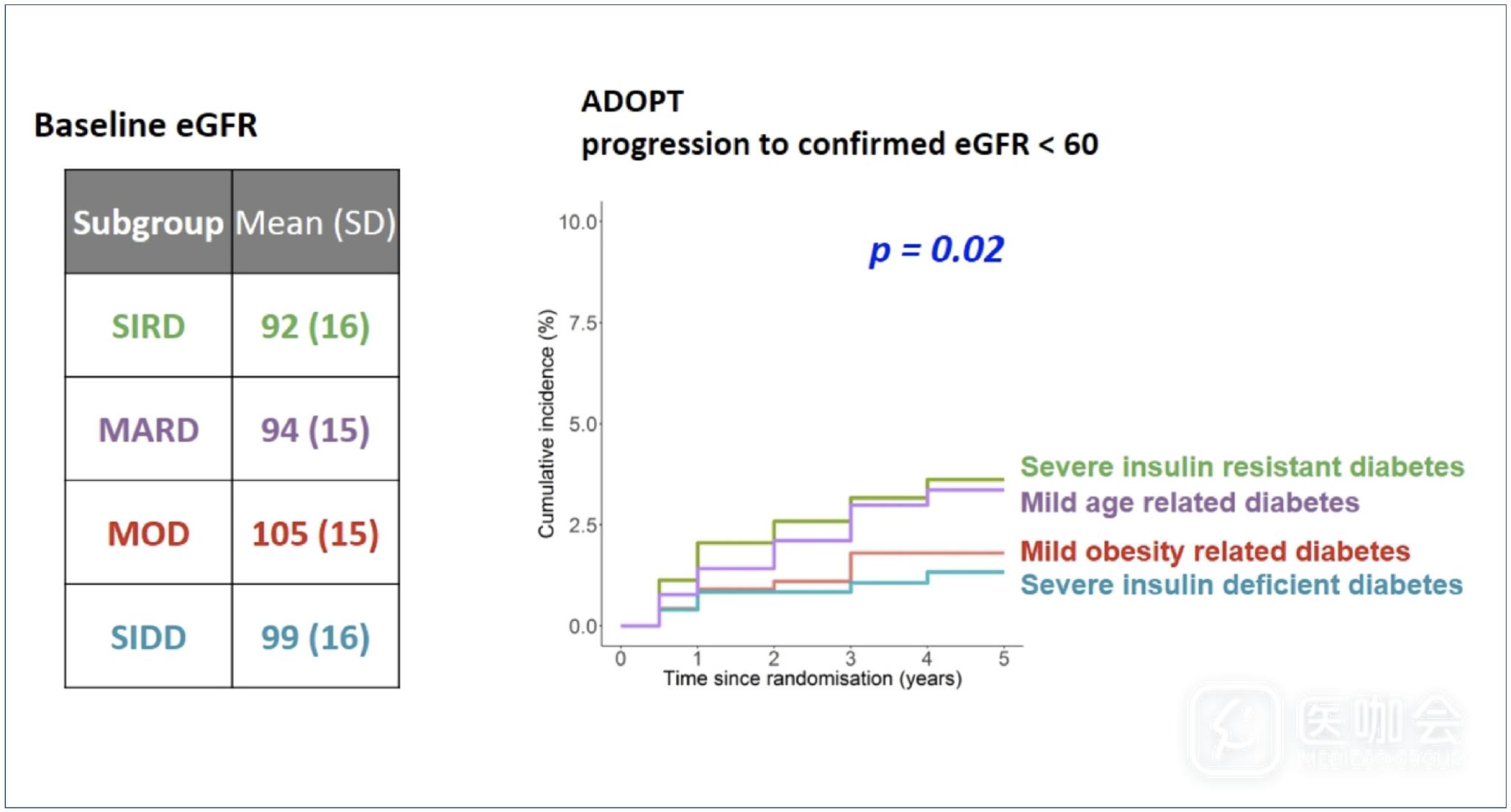
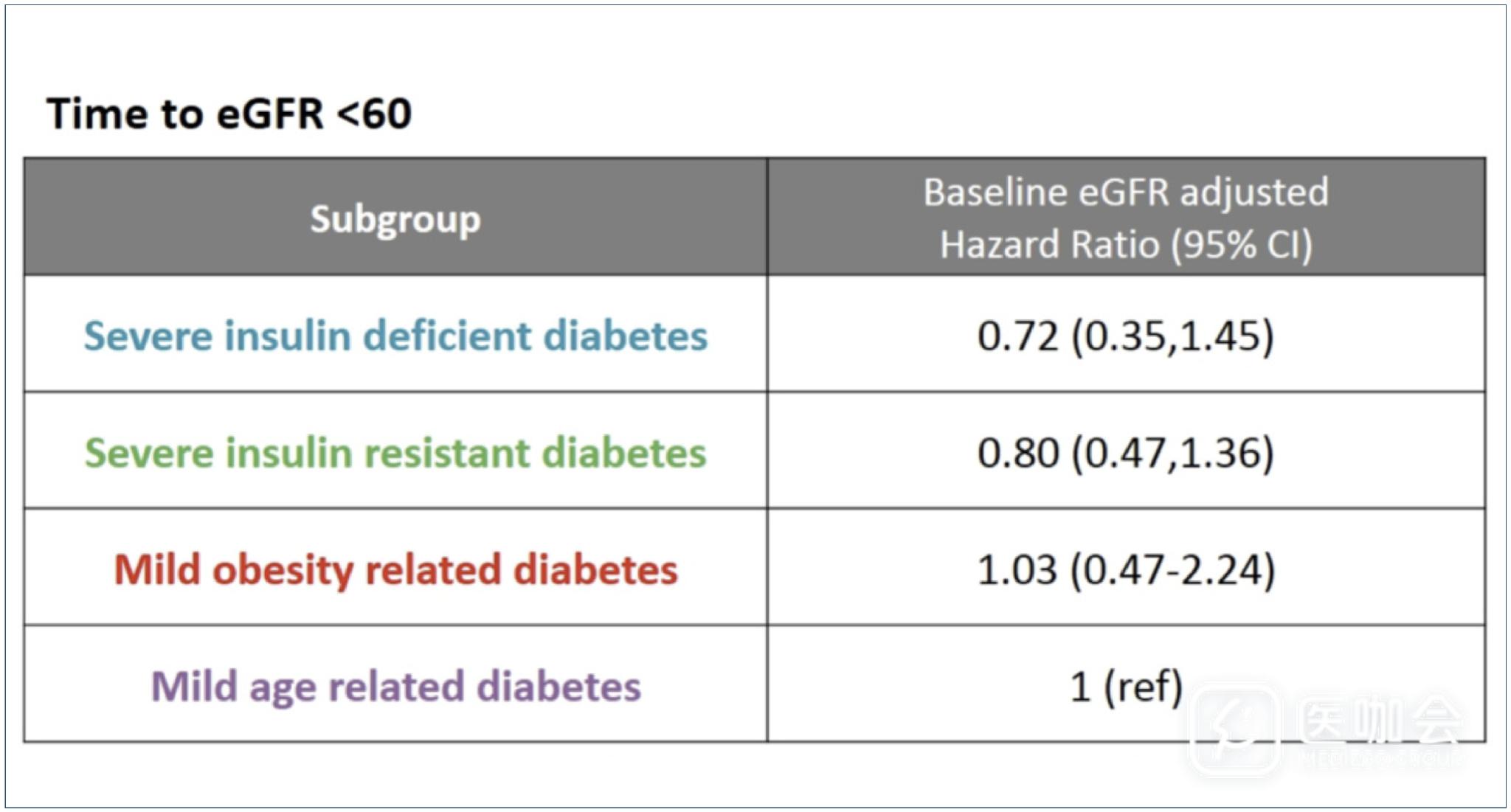
ADOPT研究中各亚型肾病的进展速度呈现明显不同【图5】,但是在排除基线eGFR<60的人群后,各组之间的这种差异明显减小【图6】,而且在进一步对各组的eGFR水平进行匹配后,各组之间的肾病进展速度并没有不同【图7】。
- SIDD:HR 0.72( 95% CI 0.35-1.45)
- SIRD:HR 0.80(95% CI 0.47-1.36)
- MOD:HR 1.03(95% CI 0.47-2.24)
- MARD:HR 1 (ref)
图5. ADOPT研究中各亚型【eGFR<60】的累计发生率
图6. 排除基线eGFR<60的人群后,各亚型【eGFR<60】的累计发生率
图7. 各组的eGFR水平进行匹配后,各组之间的肾病进展速度
4. 药物疗效的预测
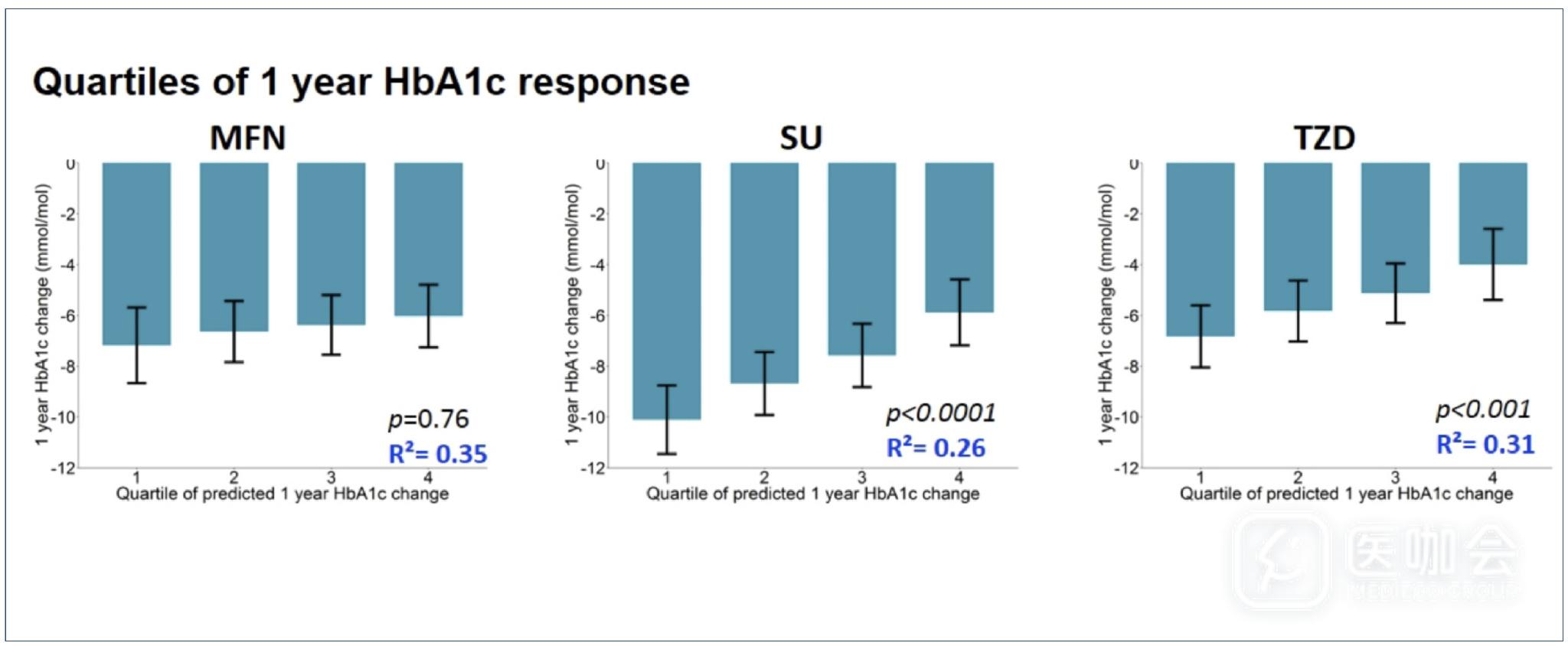
ADOPT研究中的亚型分类能否预测药物的疗效,并和简单临床指标的预测能力进行了比较,结果发现二者均能区分出不同治疗的疗效效果【除二甲双胍】,但前者的区分度并不高【图8 SU和TZD仅分别在MARD和SIRD中降糖疗效最好,其它组差别不大】,但是后者能更高的区分出降糖疗效的差异【图9】。
图8. ADOPT研究中各亚型分类对各种药物疗效的差异
图9. 通过简单临床指标区分降糖疗效的差异
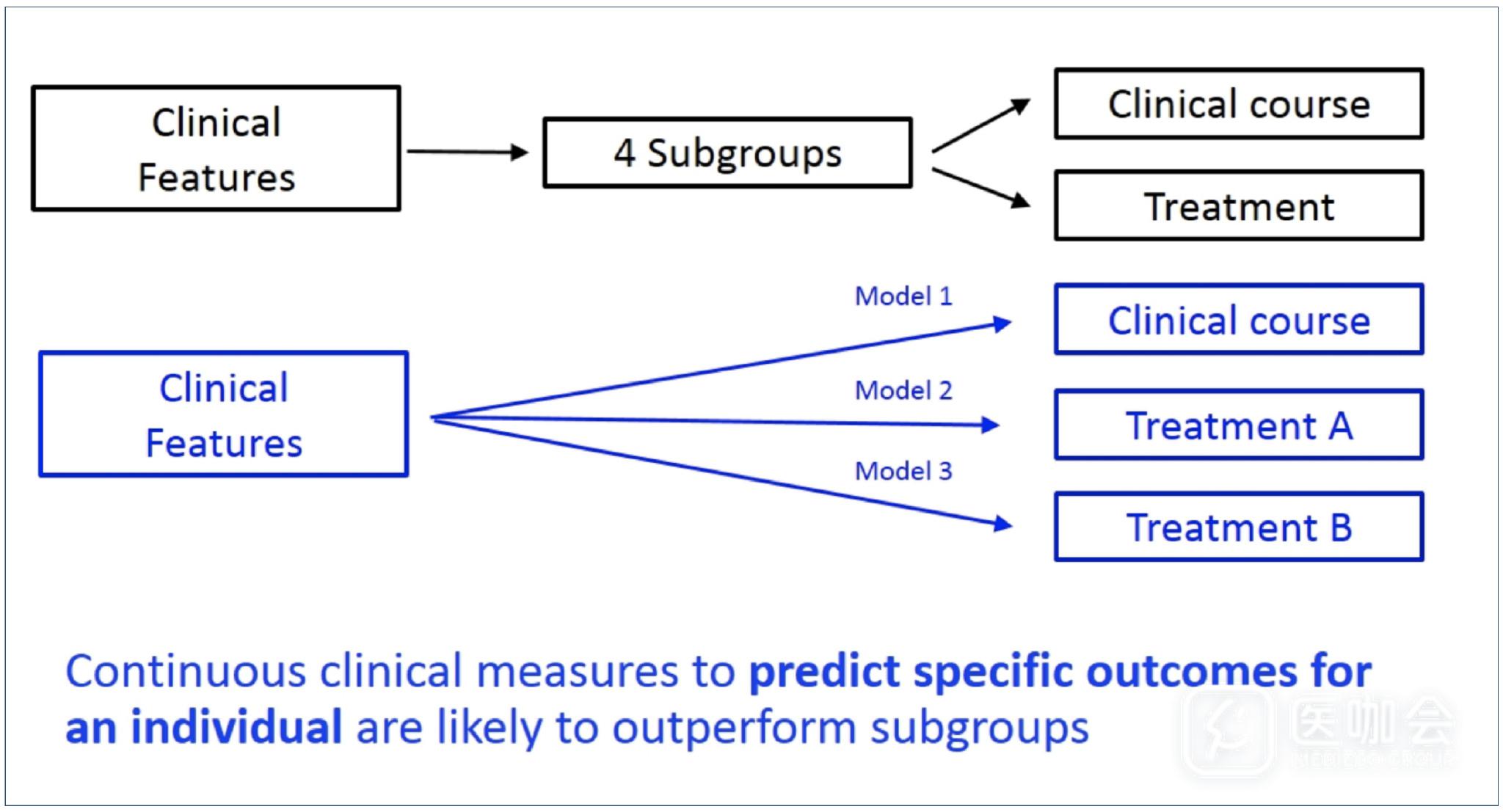
5. 总结及结论【图10】
- Alqvist教授研究中的五种亚型分类可以在大型临床试验数据中可进行重复验证。
- Alqvist教授研究中的亚型分类各组在血糖进展和治疗疗效方面存在差异。
- Alqvist教授研究中的亚型分类各组在肾脏病进展方面表现的不同原因是由于基线肾功能不同。
- Alqvist教授研究中亚型分类在在预测疾病进展和治疗疗效方面要差于连续的临床指标测量【如诊断年龄,性别,BMI,基线HbA1C】
图10