药物从研发到上市的流程(3)-临床试验及新药申请
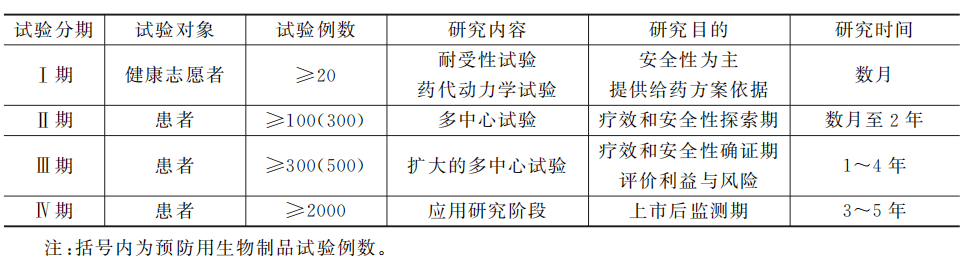
候选药物通过了临床前评价,能否上市则由临床试验结果最终加以判定。由于临床前试验模型与人体疾病真实性存在差异,对动物有效、毒副作用小的候选药物,对人体的效应并不一定相同,而且在临床试验中淘汰率较高。完成Ⅰ、Ⅱ、Ⅲ期临床试验后,可提出新药申请(new drug application, NDA)。如果研究及试验数据等能够充分证明药物安全性、有效性和质量稳定可控并通过综合审评后,NMPA核准、颁发 《药品注册批件》及附件,新药即可生产上市。
转自: https://mp.weixin.qq.com/s/JqTGvqOd3vnTZf10SEcrLg
