主要研究终点取决于试验要解决的研究目的,有时限于条件,对研究终点的选择不当,或因为诸多的不确定性,无法在试验前确定最优的主要研究终点,导致试验无法达到研究目的,或无法最大化试验的产出价值。
适应性设计中,可以在保证试验统计学严谨性以及试验整体性的前提下,根据不断积累的信息或试验外部信息调整主要终点,降低试验的风险,优化试验的产出。常见该类设计类型是由非劣效终点改变为优效性终点,如EXAMINE试验[1]:
在美国,任何降糖药上市前必须证明其不会增加重要心血管事件的风险。具体来讲,需要通过3期非劣效临床试验证明降糖药相对于标准治疗,引起重要心血管不良事件的HR 置信区间上限不超过1.3。EXAMINE试验正是这样一个非劣效3期临床试验,用于验证阿格列汀(alogliptin)是否符合上市要求。该试验入组了5380人,最终HR置信区间上限为1.16。
如果该试验的HR置信区间上限小于1,那么该试验就可以证明阿格列汀的优效性。也就是说,该试验设计可以证明阿格列汀比对照好,而不是仅仅证明非劣,但是证明优效性需要更多的样本量。下表给出了把握度为90%时要证明优效性所需要的样本量。
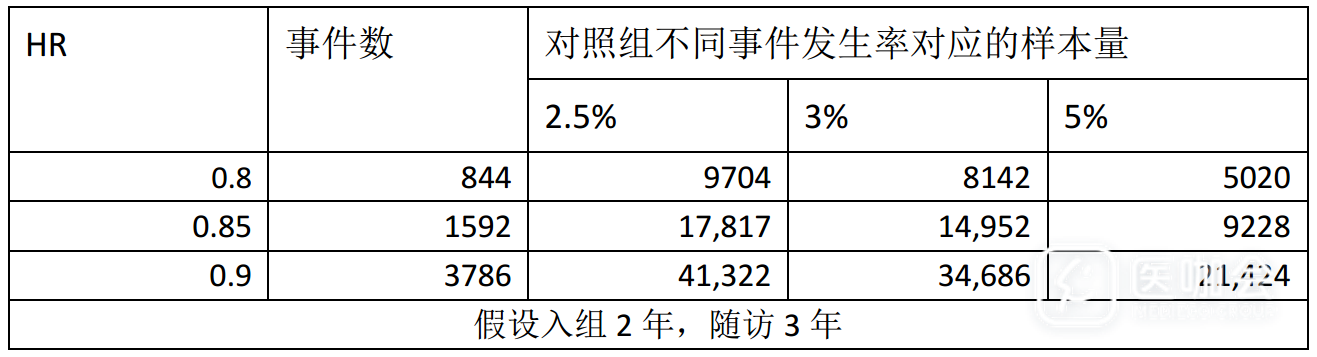
表1. 不同HR下证明优效性所需样本量
证明优效性所需样本量要比同样假设条件下证明非劣效大得多。如果试验在证明非劣效后继续使用已有的数据证明优效性,则可以在保证试验能够有充足把握度证明非劣效的前提下,额外获得证明优效性的机会,这种设计与单纯证明优效性相比无疑大大降低了试验失败的风险。
EXAMINE试验采用了改变主要研究终点的设计,主要研究终点为复合终点,包括心血管疾病导致的死亡、非致死性心肌梗死以及非致死性卒中。














确认删除